Benson-Methode: Unterschied zwischen den Versionen
- Wikipedia:Vorlagenfehler/Vorlage:Literatur/Parameterfehler
- Wikipedia:Vorlagenfehler/Vorlage:Cite journal/Parameter language fehlt
- Wikipedia:Defekte Weblinks/Ungeprüfte Archivlinks 2018-08
- Thermodynamisches Modell
imported>Leyo K (format) |
imported>Wruedt K (Abschnittlink korrigiert) |
||
| Zeile 1: | Zeile 1: | ||
{{Dieser Artikel|behandelt ein chemisches Thema. Zu der gleichnamigen Meditationstechnik siehe den Artikel [[Benson-Meditation]]}} | {{Dieser Artikel|behandelt ein chemisches Thema. Zu der gleichnamigen Meditationstechnik siehe den Artikel [[Benson-Meditation]]}} | ||
Die '''Benson-Methode''' ist eine Methode zur Abschätzung der [[Bildungsenthalpie#Standardbildungsenthalpie|Bildungsenthalpie]], [[Entropie (Thermodynamik)|Bildungsentropie]] und [[Wärmekapazität]] von Stoffen in der [[Ideales Gas|idealen Gasphase]]. Die Methode wurde von dem amerikanischen Chemiker [[Sidney Benson]] (1918–2011)<ref>Sidney William Benson (26. September 1918 – 30. Dezember 2011)</ref> im Jahr 1958 entwickelt,<ref>{{cite journal | Die '''Benson-Methode''' ist eine Methode zur Abschätzung der [[Bildungsenthalpie#Standardbildungsenthalpie|Bildungsenthalpie]], [[Entropie (Thermodynamik)|Bildungsentropie]] und [[Wärmekapazität]] von Stoffen in der [[Ideales Gas|idealen Gasphase]]. Die Methode wurde von dem amerikanischen Chemiker [[Sidney Benson]] (1918–2011)<ref>Sidney William Benson (26. September 1918 – 30. Dezember 2011)</ref> im Jahr 1958 entwickelt,<ref>{{cite journal | ||
| author | |author = Sidney W. Benson and Jerry H. Buss | ||
| date | |date = | ||
| year | |year = 1958 | ||
| month | |month = September | ||
| title | |title = Additivity Rules for the Estimation of Molecular Properties. Thermodynamic Properties | ||
| journal | |journal = [[Journal of Chemical Physics|J. Chem. Phys.]] | ||
| volume | |volume = '''29''' | ||
| issue | |issue = | ||
| pages | |pages = 546–572 (1958) | ||
| doi | |doi = 10.1063/1.1744539 | ||
| url | |url = | ||
}}</ref> später mit modernen Rechenprogrammen weiter optimiert und für andere Aggregatzustände modifiziert.<ref name="Poling">B. E. Poling, J. M. Prausnitz, J. P. O. Connell; „[[The Properties of Gases and Liquids]]“, Fifth Edition, Mc-Graw-Hill International Editions</ref> Bereits 1976 fand die Methode Eingang in moderne Lehrbücher.<ref>T. H. Lowry and K. Schueller Richardson, [https://archive.org/stream/MechanismAndTheoryInOrganicChemistry/MechanismAndTheoryInOrganicChemistry1976-LowrySchuellerRichardson#page/n81/mode/2up Mechanism and Theory in Organic Chemistry], Verlag Harper & Row, 1. Aufl. 1976, dort Seite 71 ff (Thermochemistry).</ref> | }}</ref> später mit modernen Rechenprogrammen weiter optimiert und für andere Aggregatzustände modifiziert.<ref name="Poling">B. E. Poling, J. M. Prausnitz, J. P. O. Connell; „[[The Properties of Gases and Liquids]]“, Fifth Edition, Mc-Graw-Hill International Editions</ref> Bereits 1976 fand die Methode Eingang in moderne Lehrbücher.<ref>T. H. Lowry and K. Schueller Richardson, [https://archive.org/stream/MechanismAndTheoryInOrganicChemistry/MechanismAndTheoryInOrganicChemistry1976-LowrySchuellerRichardson#page/n81/mode/2up Mechanism and Theory in Organic Chemistry], Verlag Harper & Row, 1. Aufl. 1976, dort Seite 71 ff (Thermochemistry).</ref> | ||
| Zeile 21: | Zeile 21: | ||
Methanol besteht aus einer [[Methylgruppe]] sowie einer [[Hydroxygruppe]], die hierfür zu verwendenden Inkremente werden '''C'''-(H<sub>3</sub>)(O) und '''O'''-(H)(C) bezeichnet.<ref>[http://www.nist.gov/data/PDFfiles/jpcrd458.pdf E. S. Domalski, E. D. Hearing]; ''Estimation of the Thermodynamic Properties of C-H-N-O-S-X Compounds at 298K''. In: ''[[J Phys Chem Ref Data]]'', Vol. '''22''', 805–1159 (1993), Beispiel Methanol Seite 909.</ref> | Methanol besteht aus einer [[Methylgruppe]] sowie einer [[Hydroxygruppe]], die hierfür zu verwendenden Inkremente werden '''C'''-(H<sub>3</sub>)(O) und '''O'''-(H)(C) bezeichnet.<ref>[http://www.nist.gov/data/PDFfiles/jpcrd458.pdf E. S. Domalski, E. D. Hearing]; ''Estimation of the Thermodynamic Properties of C-H-N-O-S-X Compounds at 298K''. In: ''[[J Phys Chem Ref Data]]'', Vol. '''22''', 805–1159 (1993), Beispiel Methanol Seite 909.</ref> | ||
* Zur Berechnung der [[Bildungsenthalpie#Standardbildungsenthalpie|Bildungsenthalpie]] in der Gasphase (298 K) sind die zwei Inkremente −42,26 und −159,33 kJ/mol zu verwenden (Methanol ber. −201,59; exp. −201,10 kJ/mol). | * Zur Berechnung der [[Bildungsenthalpie#Standardbildungsenthalpie|Bildungsenthalpie]] in der Gasphase (298 K) sind die zwei Inkremente −42,26 und −159,33 kJ/mol zu verwenden (Methanol ber. −201,59; exp. −201,10 kJ/mol). | ||
* Zur Berechnung der [[Wärmekapazität# | * Zur Berechnung der [[Spezifische Wärmekapazität#Beziehungen zu Wärmekapazität und molarer Wärmekapazität|molaren Wärmekapazität]] C<sub>p</sub> werden die Inkremente 25,73 und 18,16 J/mol K verwendet (Methanol ber. 43,89, exp. 43,89 J/mol K) | ||
* Zur Berechnung der [[Entropie (Thermodynamik)|Entropie]] muss neben den Inkrementen 127,32 und 121,50 noch ein Symmetriebeitrag von −9,13 J/mol K berücksichtigt werden (Methanol ber. 239,69, exp. 239,70 J/mol K). | * Zur Berechnung der [[Entropie (Thermodynamik)|Entropie]] muss neben den Inkrementen 127,32 und 121,50 noch ein Symmetriebeitrag von −9,13 J/mol K berücksichtigt werden (Methanol ber. 239,69, exp. 239,70 J/mol K). | ||
Die Arbeit von Domalski (1993) erlaubt mit anderen Inkrement-Sätzen auch die Berechnung thermodynamischer Daten für den flüssigen und festen Aggregatzustand. | Die Arbeit von Domalski (1993) erlaubt mit anderen Inkrement-Sätzen auch die Berechnung thermodynamischer Daten für den flüssigen und festen Aggregatzustand. | ||
== Anwendung == | == Anwendung == | ||
Der eigentliche Nutzen liegt darin, für jedes beliebige Moleküle diese thermodynamischen Größen berechnen zu können. [[Enthalpie# | Der eigentliche Nutzen liegt darin, für jedes beliebige Moleküle diese thermodynamischen Größen berechnen zu können. [[Enthalpie#Enthalpie in der Chemie (Thermochemie)|Reaktionswärmen]] [[Reaktionswärme#Erläuterung|(endotherm/exotherm)]] bei chemischen Reaktionen lassen sich aus den Differenzen der Bildungsenthalpien aller Reaktanten vorzüglich abschätzen, zum Beispiel bei der Oxidation des Methanols. Bei durchgängiger Benutzung von Daten für den gasförmigen bzw. den flüssigen Zustand werden rechnerisch vergleichbare Reaktionsenthalpien erhalten ([[Hess’scher Wärmesatz]]<ref>[http://www.imn.htwk-leipzig.de/~stich/Bilder_ME/III.III.pdf Hess’scher Wärmesatz] zur Berechnung von Reaktionswärmen aus Bildungsenthalpien.</ref>) ''>>Not only is the method fairly easy to apply, but it usually can estimate properties with an uncertainty no larger than typical experimental uncertainties.<<'' (N. Cohen 1996) | ||
Referenzdaten für Standard-Bildungsenthalpien finden sich im [[CRC Handbook of Chemistry and Physics]] im Kapitel 5.4.<ref>{{Webarchiv | url=http://courses.chem.indiana.edu/c360/documents/thermodynamicdata.pdf | wayback=20150426054824 | text=STANDARD THERMODYNAMIC PROPERTIES OF CHEMICAL SUBSTANCES}}, Kapitel 5.4 aus [[CRC Handbook of Chemistry and Physics|CRC Handbook]] 90. Auflage (2009–2010).</ref> Werte für den Gaszustand und flüssigen Zustand unterscheiden sich definitionsgemäß um den Betrag der Standard-Verdampfungsenthalpie (25 °C). | Referenzdaten für Standard-Bildungsenthalpien finden sich im [[CRC Handbook of Chemistry and Physics]] im Kapitel 5.4.<ref>{{Webarchiv | url=http://courses.chem.indiana.edu/c360/documents/thermodynamicdata.pdf | wayback=20150426054824 | text=STANDARD THERMODYNAMIC PROPERTIES OF CHEMICAL SUBSTANCES}}, Kapitel 5.4 aus [[CRC Handbook of Chemistry and Physics|CRC Handbook]] 90. Auflage (2009–2010).</ref> Werte für den Gaszustand und flüssigen Zustand unterscheiden sich definitionsgemäß um den Betrag der Standard-Verdampfungsenthalpie (25 °C). | ||
| Zeile 66: | Zeile 66: | ||
Dieser Teilschritt ist mit −62 kJ/mol exotherm. | Dieser Teilschritt ist mit −62 kJ/mol exotherm. | ||
[[Datei:Synthese von Ethylenglycol (OMEGA Shell Prozess).svg|rahmenlos|hochkant=2.8|zentriert|Synthese von Ethylenglycol (OMEGA Shell Prozess)]] | |||
Im 2. Schritt wird hieran Wasser (<math>\Delta H_f^0</math>= −241,5 kJ/mol) addiert und unter Abspaltung von Kohlendioxid entsteht das [[Ethylenglycol]] (<math>\Delta H_f^0</math>= −384,5 kJ/mol). | Im 2. Schritt wird hieran Wasser (<math>\Delta H_f^0</math>= −241,5 kJ/mol) addiert und unter Abspaltung von Kohlendioxid entsteht das [[Ethylenglycol]] (<math>\Delta H_f^0</math>= −384,5 kJ/mol). | ||
| Zeile 75: | Zeile 75: | ||
: 1993 gelang es ''Domalski'', auch die Bildungsenthalpien von Stoffen in der flüssigen oder festen Phase vorherzusagen. Bei der Berechnung der Entropie in der flüssigen oder festen Phase entfällt die Berücksichtigung von Konformeren.<ref>[http://www.nist.gov/data/PDFfiles/jpcrd458.pdf E. S. Domalski, E. D. Hearing]; "Estimation of the Thermodynamic Properties of C-H-N-O-S-X Compounds at 298K", J. Phys. Chem. Ref. Data, Vol. '''22''', 805–1159 (1993)</ref> | : 1993 gelang es ''Domalski'', auch die Bildungsenthalpien von Stoffen in der flüssigen oder festen Phase vorherzusagen. Bei der Berechnung der Entropie in der flüssigen oder festen Phase entfällt die Berücksichtigung von Konformeren.<ref>[http://www.nist.gov/data/PDFfiles/jpcrd458.pdf E. S. Domalski, E. D. Hearing]; "Estimation of the Thermodynamic Properties of C-H-N-O-S-X Compounds at 298K", J. Phys. Chem. Ref. Data, Vol. '''22''', 805–1159 (1993)</ref> | ||
: 1996 wurden von ''Cohen'' Werte für die Berechnung der Enthalpie in allen drei Phasen publiziert, welche die Genauigkeit der Werte von Domalski teilweise übersteigen.<ref>[http://www.nist.gov/data/PDFfiles/jpcrd513.pdf N. Cohen]; "Revised Group Additivity Values for Enthalpies of Formation (at 298 K) of C-H and C-H-O Compounds", J. Phys. Chem. Ref. Data, Vol. '''25''', 1411–1481 (1996)</ref> | : 1996 wurden von ''Cohen'' Werte für die Berechnung der Enthalpie in allen drei Phasen publiziert, welche die Genauigkeit der Werte von Domalski teilweise übersteigen.<ref>[http://www.nist.gov/data/PDFfiles/jpcrd513.pdf N. Cohen]; "Revised Group Additivity Values for Enthalpies of Formation (at 298 K) of C-H and C-H-O Compounds", J. Phys. Chem. Ref. Data, Vol. '''25''', 1411–1481 (1996)</ref> | ||
: ''Salmon'' und ''Dalmazzone'' veröffentlichten ab 2006 Gruppenbeiträge für die Bildungsenthalpie von Feststoffen.<ref> | : ''Salmon'' und ''Dalmazzone'' veröffentlichten ab 2006 Gruppenbeiträge für die Bildungsenthalpie von Feststoffen.<ref>; "Prediction of Enthalpy of Formation in the Solid Phase (at 298 K) using Second-Order Group Contributions – Part I: C-H and C-H-O Compounds", J. Phys. Chem. Ref. Data, Vol. '''35''', 1443–1457 (2006). – {{Webarchiv|url=http://scitation.aip.org/content/aip/journal/jpcrd/36/1/10.1063/1.2435401 |wayback=20140329202107 |text=A. Salmon, D. Dalmazzone |archiv-bot=2018-08-28 23:41:02 InternetArchiveBot }}; "Prediction of Enthalpy of Formation in the Solid State (at 298 K) Using Second-Order Group Contributions — Part II: C-H, C-H-O, and C-H-N-O Compounds", J. Phys. Chem. Ref. Data, Vol. '''36''', 19–58 (2007)</ref> | ||
== Weblinks == | |||
* [http://srdata.nist.gov/gateway/gateway?keyword=enthalpy+of+formation NIST-Literaturübersicht zu "Bildungsenthalpien"]. – N. Cohen (1996) erhielt von NIST den Auftrag zur Validierung und Optimierung der Inkremente sowie Benennung von Referenzwerten. | |||
== Einzelnachweise == | == Einzelnachweise == | ||
<references /> | <references /> | ||
[[Kategorie:Thermodynamisches Modell]] | [[Kategorie:Thermodynamisches Modell]] | ||
Aktuelle Version vom 26. April 2020, 09:31 Uhr
Die Benson-Methode ist eine Methode zur Abschätzung der Bildungsenthalpie, Bildungsentropie und Wärmekapazität von Stoffen in der idealen Gasphase. Die Methode wurde von dem amerikanischen Chemiker Sidney Benson (1918–2011)[1] im Jahr 1958 entwickelt,[2] später mit modernen Rechenprogrammen weiter optimiert und für andere Aggregatzustände modifiziert.[3] Bereits 1976 fand die Methode Eingang in moderne Lehrbücher.[4]
Prinzip
Die Methode basiert auf der Annahme, dass jedes Atom eines Moleküls einen spezifischen Beitrag zu den thermodynamischen Eigenschaften eines Moleküls beiträgt. Die Bindungstypen aller Atome müssen hierfür prinzipiell bekannt sein, räumliche Geometrien (strukturelle Isomere, Konformere/Rotamere und Symmetrien) führen nur zu kleineren Sonderbeiträgen bei der Kumulation der Inkremente (Einzelbeiträge).[3]
Systematik am Beispiel Methanol
Methanol besteht aus einer Methylgruppe sowie einer Hydroxygruppe, die hierfür zu verwendenden Inkremente werden C-(H3)(O) und O-(H)(C) bezeichnet.[5]
- Zur Berechnung der Bildungsenthalpie in der Gasphase (298 K) sind die zwei Inkremente −42,26 und −159,33 kJ/mol zu verwenden (Methanol ber. −201,59; exp. −201,10 kJ/mol).
- Zur Berechnung der molaren Wärmekapazität Cp werden die Inkremente 25,73 und 18,16 J/mol K verwendet (Methanol ber. 43,89, exp. 43,89 J/mol K)
- Zur Berechnung der Entropie muss neben den Inkrementen 127,32 und 121,50 noch ein Symmetriebeitrag von −9,13 J/mol K berücksichtigt werden (Methanol ber. 239,69, exp. 239,70 J/mol K).
Die Arbeit von Domalski (1993) erlaubt mit anderen Inkrement-Sätzen auch die Berechnung thermodynamischer Daten für den flüssigen und festen Aggregatzustand.
Anwendung
Der eigentliche Nutzen liegt darin, für jedes beliebige Moleküle diese thermodynamischen Größen berechnen zu können. Reaktionswärmen (endotherm/exotherm) bei chemischen Reaktionen lassen sich aus den Differenzen der Bildungsenthalpien aller Reaktanten vorzüglich abschätzen, zum Beispiel bei der Oxidation des Methanols. Bei durchgängiger Benutzung von Daten für den gasförmigen bzw. den flüssigen Zustand werden rechnerisch vergleichbare Reaktionsenthalpien erhalten (Hess’scher Wärmesatz[6]) >>Not only is the method fairly easy to apply, but it usually can estimate properties with an uncertainty no larger than typical experimental uncertainties.<< (N. Cohen 1996)
Referenzdaten für Standard-Bildungsenthalpien finden sich im CRC Handbook of Chemistry and Physics im Kapitel 5.4.[7] Werte für den Gaszustand und flüssigen Zustand unterscheiden sich definitionsgemäß um den Betrag der Standard-Verdampfungsenthalpie (25 °C).
Reaktionsenthalpie Oxidation von Methanol
Die Bildungsenthalpie $ \Delta H_{f}^{0} $ von Methanol ist −201,6 kJ/mol. Bei der Oxidation bilden sich Formaldehyd ($ \Delta H_{f}^{0} $= −108,6 kJ/mol) und Wasser ($ \Delta H_{f}^{0} $= −241,5 kJ/mol), der Prozess in der Gasphase ist stark exotherm (ber. −148 kJ/mol).[8]
Reaktionsenthalpie Hydratation von Formaldehyd
Leitet man das Formaldehydgas ($ \Delta H_{f}^{0} $= −108,6 kJ/mol) in Wasser ($ \Delta H_{f}^{0} $= −241,5 kJ/mol), so bildet sich das Hydrat (ber. $ \Delta H_{f}^{0} $= −380,9 kJ/mol). Diese Hydratisierung ist schwach exotherm, das Gleichgewicht liegt fast vollständig auf der Seite des Aldehydhydrats.
Reaktionsenthalpie Dehydrierung von Methylcyclohexan
Das Erhitzen von Methylcyclohexan (ber. $ \Delta H_{f}^{0} $= −149,2 kJ/mol) mit Hydrier/Dehydrierkatalysatoren ergibt unter Wasserstoff-Abspaltung Toluol (ber. $ \Delta H_{f}^{0} $= +50,4 kJ/mol). Die Reaktion ist stark endotherm (ber. +200 kJ/mol).[9]
Die Umkehrung dieser Reaktion, die Hydrierung von aromatischen Kohlenwasserstoffen, setzt hohe Wärmemengen frei. Dies ist bedeutsam bei Prüfung von Dibenzyltoluol auf Eignung als flüssiger organischer Wasserstoffträger.
Reaktionsenthalpie Hydrolyse von Ethylenoxid
Bei der Addition von Wasser ($ \Delta H_{f}^{0} $= −241,5 kJ/mol) an Ethylenoxid (ber. $ \Delta H_{f}^{0} $= −52,6 kJ/mol) bei 200 °C oder unter Säurekatalyse in Wasser, so bildet sich u. a. Ethylenglycol (ber. $ \Delta H_{f}^{0} $= −384,5 kJ/mol). Die Reaktion ist wie beim homologen Propylenoxid stark exotherm (ber. −90 kJ/mol).[10]
Die Ringöffnungsreaktionen mit Aminen (z. B. "Epoxy-Amin-Additionen" bei 2K-Klebern) sind vergleichbar exotherm.
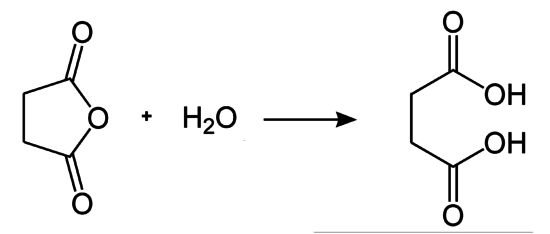
Reaktionsenthalpie Hydrolyse von Bernsteinsäureanhydrid
Bei der Addition von Wasser ($ \Delta H_{f}^{0} $= −241,5 kJ/mol) an Bernsteinsäureanhydrid (ber. $ \Delta H_{f}^{0} $= −527,9 kJ/mol) bildet sich Bernsteinsäure (ber. $ \Delta H_{f}^{0} $= −826,8 kJ/mol). Die Reaktion ist exotherm (ber. −57 kJ/mol).[11] Für die Hydrolyse von Maleinsäureanhydrid wird mit −53 kJ/mol eine vergleichbare Wärmetönung wie für Acetanhydrid oder Phthalsäureanhydrid berechnet.
Carbonatisierung von Ethylenoxid und Hydrolyse des Ethylencarbonats (OMEGA-Prozess)
Bei der Addition von Kohlendioxid ($ \Delta H_{f}^{0} $= −393,5 kJ/mol) an Ethylenoxid (ber. $ \Delta H_{f}^{0} $= −52,6 kJ/mol) bildet sich Ethylencarbonat ($ \Delta H_{f}^{0} $= −508,5 kJ/mol).
Dieser Teilschritt ist mit −62 kJ/mol exotherm.
Im 2. Schritt wird hieran Wasser ($ \Delta H_{f}^{0} $= −241,5 kJ/mol) addiert und unter Abspaltung von Kohlendioxid entsteht das Ethylenglycol ($ \Delta H_{f}^{0} $= −384,5 kJ/mol).
Der 2. Teilschritt ist mit −28 kJ/mol deutlich schwächer exotherm.
Weiterentwicklungen
Die Benson-Methode wurde in der Folge auch vor dem Hintergrund leistungsfähiger Computersysteme von mehreren Physikochemikern weiterentwickelt.
- 1993 gelang es Domalski, auch die Bildungsenthalpien von Stoffen in der flüssigen oder festen Phase vorherzusagen. Bei der Berechnung der Entropie in der flüssigen oder festen Phase entfällt die Berücksichtigung von Konformeren.[12]
- 1996 wurden von Cohen Werte für die Berechnung der Enthalpie in allen drei Phasen publiziert, welche die Genauigkeit der Werte von Domalski teilweise übersteigen.[13]
- Salmon und Dalmazzone veröffentlichten ab 2006 Gruppenbeiträge für die Bildungsenthalpie von Feststoffen.[14]
Weblinks
- NIST-Literaturübersicht zu "Bildungsenthalpien". – N. Cohen (1996) erhielt von NIST den Auftrag zur Validierung und Optimierung der Inkremente sowie Benennung von Referenzwerten.
Einzelnachweise
- ↑ Sidney William Benson (26. September 1918 – 30. Dezember 2011)
- ↑ Sidney W. Benson and Jerry H. Buss: Additivity Rules for the Estimation of Molecular Properties. Thermodynamic Properties. In: J. Chem. Phys. 29 . Jahrgang, September 1958, S. 546–572 (1958), doi:10.1063/1.1744539.
- ↑ 3,0 3,1 B. E. Poling, J. M. Prausnitz, J. P. O. Connell; „The Properties of Gases and Liquids“, Fifth Edition, Mc-Graw-Hill International Editions
- ↑ T. H. Lowry and K. Schueller Richardson, Mechanism and Theory in Organic Chemistry, Verlag Harper & Row, 1. Aufl. 1976, dort Seite 71 ff (Thermochemistry).
- ↑ E. S. Domalski, E. D. Hearing; Estimation of the Thermodynamic Properties of C-H-N-O-S-X Compounds at 298K. In: J Phys Chem Ref Data, Vol. 22, 805–1159 (1993), Beispiel Methanol Seite 909.
- ↑ Hess’scher Wärmesatz zur Berechnung von Reaktionswärmen aus Bildungsenthalpien.
- ↑ STANDARD THERMODYNAMIC PROPERTIES OF CHEMICAL SUBSTANCES (Memento vom 26. April 2015 im Internet Archive), Kapitel 5.4 aus CRC Handbook 90. Auflage (2009–2010).
- ↑ Bildungsenthalpien Methanol und Formaldehyd siehe Domalski 1993, Seiten 935 und 909, Ber. aus Inkremente und exp. Werte.
- ↑ Bildungsenthalpien Methylcyclohexan und Toluol siehe Domalski 1993, Seiten 863 und 896, Ber. aus Inkremente und exp. Werte.
- ↑ Bildungsenthalpien Ethylenoxid und Ethylenglycol siehe Domalski 1993, Seiten 932 und 917, Ber. aus Inkremente und exp. Werte.
- ↑ Bildungsenthalpien Bernsteinsäureanhydrid und Bernsteinsäure siehe Domalski 1993, Seiten 964 und 951, Ber. aus Inkremente und exp. Werte.
- ↑ E. S. Domalski, E. D. Hearing; "Estimation of the Thermodynamic Properties of C-H-N-O-S-X Compounds at 298K", J. Phys. Chem. Ref. Data, Vol. 22, 805–1159 (1993)
- ↑ N. Cohen; "Revised Group Additivity Values for Enthalpies of Formation (at 298 K) of C-H and C-H-O Compounds", J. Phys. Chem. Ref. Data, Vol. 25, 1411–1481 (1996)
- ↑ ; "Prediction of Enthalpy of Formation in the Solid Phase (at 298 K) using Second-Order Group Contributions – Part I: C-H and C-H-O Compounds", J. Phys. Chem. Ref. Data, Vol. 35, 1443–1457 (2006). – A. Salmon, D. Dalmazzone (Memento des Originals vom 29. März 2014 im Internet Archive) Info: Der Archivlink wurde automatisch eingesetzt und noch nicht geprüft. Bitte prüfe Original- und Archivlink gemäß Anleitung und entferne dann diesen Hinweis.; "Prediction of Enthalpy of Formation in the Solid State (at 298 K) Using Second-Order Group Contributions — Part II: C-H, C-H-O, and C-H-N-O Compounds", J. Phys. Chem. Ref. Data, Vol. 36, 19–58 (2007)